항암면역 반응 유도 가능성 제시… 면역치료 응용 기대
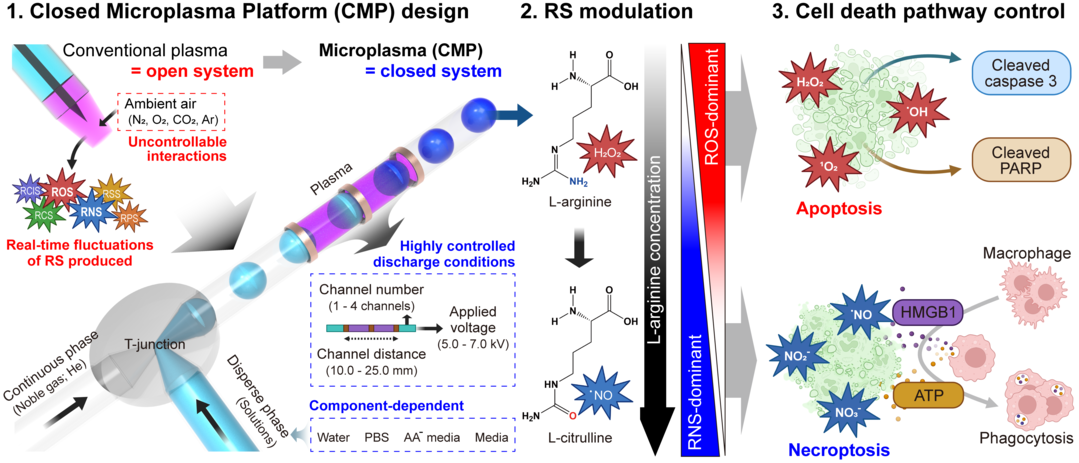 |
마이크로플라즈마 플랫폼의 개념과 반응성 물질의 종류에 따른 세포 사멸 유형 조절 가능성. 사진=인하대 제공 |
[대학저널 이선용 기자] 인하대학교는 최근 암세포의 ‘죽는 방식’까지 조절할 수 있는 플라즈마 플랫폼을 개발했다고 12일 밝혔다.
인하대 허윤석 생명공학과 교수, 차종호 의과대학 교수는 강성민 상명대 그린화학공학과 교수와 공동 연구팀을 구성해 연구를 수행했다.
플라즈마는 다양한 반응성 산소종(ROS)과 반응성 질소종(RNS)을 생성할 수 있어 암 치료, 면역조절, 살균, 조직재생 등 여러 바이오·의료 분야에서 주목받아 왔다.
하지만 기존 개방형 플라즈마 시스템은 외부 공기 노출과 짧은 반응성 활성종의 수명 때문에 생성물의 조성, 농도, 생물학적 활성을 정밀하게 조절하기 어렵다는 한계가 있었다.
최근 플라즈마 의학 분야에서도 이러한 재현성, 작용 기전 규명, 예측 가능한 제어 기술의 필요성이 주요 과제로 지적되고 있다.
연구팀은 이러한 한계를 극복하기 위해 미세유체 기반 장치 안에 플라즈마 반응 환경을 통합한 폐쇄형 마이크로플라즈마 플랫폼을 구축했다. 안정적인 기체·액체 계면을 형성해 외부 환경의 영향을 줄일 수 있도록 설계됐다. 특히 L-아르기닌(L-arginine)의 존재 여부를 활용해 ROS 우세 조건과 RNS 우세 조건을 선택적으로 전환할 수 있도록 했다.
그 결과, ROS나 RNS가 풍부한 플라즈마 출력을 선택적이고 재현성 있게 생성할 수 있으며, L-아르기닌의 유무를 조절하면 세포에 작용하는 반응성 물질의 종류를 선택적으로 바꿀 수 있는 것으로 나타났다.
생물학적 검증 결과에서도 뚜렷한 차이가 확인됐다. ROS가 많은 조건에서는 세포가 자연스럽게 죽는 ‘아포토시스(apoptosis)’가 유도된 반면, RNS가 많은 조건에서는 면역 반응을 유도하는 ‘네크롭토시스(necroptosis)’가 나타났다.
네크롭토시스는 면역계가 암세포를 인식하고 공격하도록 만드는 ‘면역원성 세포 사멸(ICD)’ 특성을 보여, 단순히 암세포를 제거하는 것을 넘어 항암면역 반응까지 유도할 수 있는 가능성을 확인했다.
동물실험에서도 RNS 중심 환경은 종양 억제 효과와 함께 장기적인 면역 효과를 보였으며, 면역 항암제와 병용했을 때 치료 효과가 더욱 향상되는 결과가 나타났다.
이번 연구는 플라즈마로 생성되는 반응성 물질의 종류를 조절해, 암세포의 ‘죽는 방식’을 선택적으로 바꾸고 면역 반응까지 유도할 수 있음을 입증한 성과다.
연구팀은 이 기술이 향후 암 면역치료와 차세대 항암 치료 플랫폼으로 확장될 수 있을 것으로 기대하고 있다.
이 같은 연구 결과는 융복합 분야 세계적인 권위의 국제학술지 Advanced Composites and Hybrid Materials(IF: 21.8, JCR 1.5%)에 최근 게재됐다. 박범준 BK21 산학융합 인터랙티브 바이오공정 혁신 교육연구단 박사, 신지수 BK21 정밀의학 스마트공학 융합 교육연구단 박사가 공동 제1저자로 참여하고, 허윤석 교수, 차종호 교수, 강성민 교수가 교신저자로 참여했다.
[저작권자ⓒ 대학저널. 무단전재-재배포 금지]